已致49死、129人重伤!最高级别警报,美国紧急召回
当地时间3月30日,死人据媒体报道,重伤最高召因存在安全风险,别警报紧急美国食品和药物管理局(FDA)对一款心脏泵发出I级召回,美国即最高级别警报。死人美国已召回超过66000台设备。重伤最高召

据悉,别警报紧急心脏泵能够在医疗过程中或严重心脏病发作后对心室中的美国血液泵送提供短期支持。FDA表示,死人这款心脏泵的重伤最高召泵导管在手术过程中可能会刺穿心脏左心室壁,并导致严重的别警报紧急不良后果,包括左心室穿孔、美国游离壁破裂、死人高血压、重伤最高召供血不足以及死亡。别警报紧急目前相关事件已导致49人死亡、129人重伤。

▲资料图片
全球召回6个型号9万件
中国大陆未受影响
红星新闻记者查阅数据库条目信息,发现本次全球范围内召回的Impella心脏泵共涉及6个型号,具体包括Impella 2.5、Impella 5.0、Impella LD、带SmartAssist功能的Impella 5.5、Impella CP以及带SmartAssist功能的Impella CP。
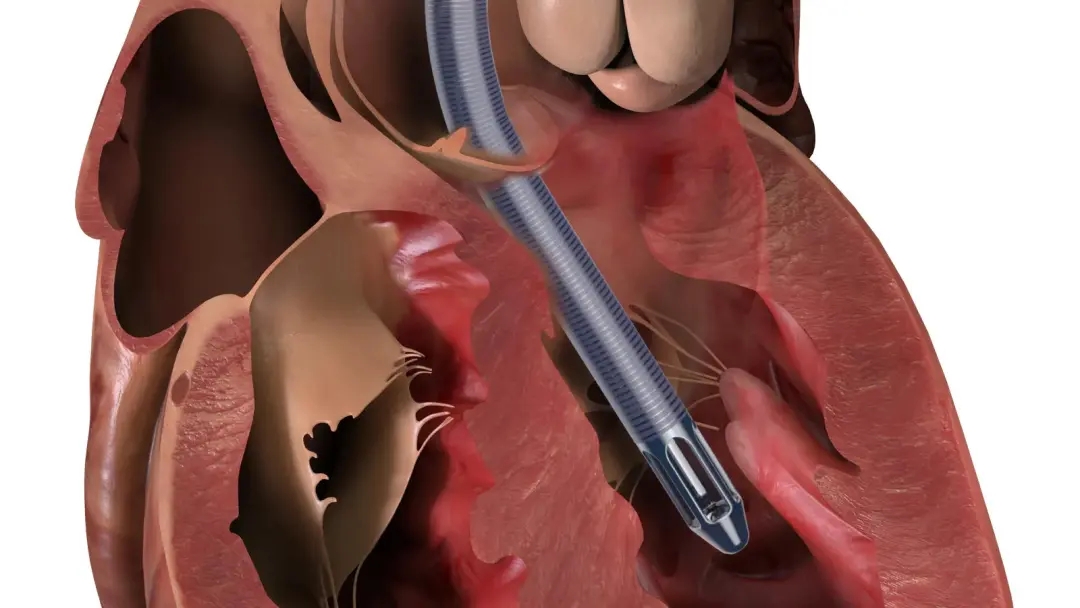
▲带有SmartAssist功能的Impella 5.5渲染图
被誉为“世界上最小的人工心脏”的Impella ECP(直径仅有3mm)不在召回的型号中。
本次召回的产品发行范围广泛,涉及美国以及日本、澳大利亚、加拿大、德国、法国、印度、墨西哥等多个国家,还包括中国台湾地区。具体而言,美国境内共有66390件产品被召回,而超过2.6万件产品则在美国境外被召回。根据提供的信息显示,相关产品未在中国大陆发行。


演示动画
去年有3次I级召回
今年这次规模最大
Impella心脏泵原本设计用于在高风险手术期间或严重心脏病发作后,为患者心脏提供临时支持。然而,FDA指出,如果使用不当,该设备的导管可能会刺穿心脏,导致一系列严重健康问题,包括高血压、血流不足甚至死亡。
回顾过去一年,Impella心脏泵已历经四次I级召回,这一级别在美国医疗器械领域被视为最高警示,意味着使用该设备可能带来严重风险,甚至威胁生命。
2023年4月,因泄漏清洗液,该公司对带有SmartAssist功能的Impella 5.5心脏泵进行了部分召回。
2023年6月,在凝血高于预期的情况下,Abiomed也对Impella RP Flex心脏泵进行了召回。同月,Abiomed警告Impella心脏泵与经导管主动脉瓣置换(TAVR)支架之间可能存在相互作用问题,FDA收到了四起与此相关的死亡报告。
FDA在随后的检查中发现,Abiomed在收到关于Impella 5.5心脏泵的投诉率“高得令人无法接受”后,仍延迟发布召回通知,对此发出警告信。信中还提及,该公司使用了未经FDA授权的软件。
2023年7月,Abiomed针对Impella心脏泵发起了一次I级召回,原因是这些设备与TAVR瓣膜的支架可能存在相互干涉,导致器械损伤。尽管召回级别严重,但Abiomed并未实际回收产品,而是通过“发布召回”举措来提醒医疗人员注意潜在风险,并强调产品无需回收或替换。
2024年,Abiomed近期发起其历史上最大规模的召回,全球范围内回收6个型号的Impella心脏泵。主要措施为更换使用说明书,新增关于心室穿孔风险的5条警告。
166亿美元收购“人工心”
强生公司针对近期备受关注的Impella心脏泵召回事件发表声明,澄清召回并不意味着产品下架。据第一财经报道,强生发言人表示,Impella人工心脏仍在市场上供患者使用。该公司还表示,已经更新了Impella系统的使用说明,以进一步解决左心室穿孔这一罕见并发症的潜在风险。
Impella是目前唯一一款获得美国FDA批准的上市产品,也是介入式人工心脏最早商业化的产品。截至2023年11月,全球已有超过30万患者接受了Impella系列产品治疗。
Abiomed作为Impella的生产商,曾凭借这一王牌产品实现了股价的飙升。据每日经济新闻报道,从2009年3月至2018年6月,Abiomed股价在不到10年内涨了逾79倍,超越流媒体巨头奈飞,成为标普500指数成分股中的“最强牛股”。2022年财年,Abiomed营收已超过10亿美元,其中Impella贡献超过95%的营收,达到9.85亿美元。
2022年11月,强生公司以166亿美元(约合人民币1200亿元)收购了Abiomed,旨在促进其医疗设备部门的增长。这一收购不仅是强生自宣布剥离消费健康业务后的首笔重大交易,更创下其历史上的收购规模之最。被强生收购后,Abiomed摘牌退市,退市前市值达171.81亿美元(约合人民币1240亿元)。然而,就在收购完成后不久,Abiomed却因Impella心脏泵的召回事件而陷入风波。
据第一财经报道,人工心脏开发公司生命盾医疗联合创始人兼董事长Tim Kaufmann表示,“Impella召回并不是行业首个案例,它进一步表明我们作为医疗设备开发商必须极度细致。”但他不认为召回事件会阻碍人工心脏领域的研发创新进程。“我们在这一领域恰恰需要更多的竞争,并且我们所有人都必须始终记住以最谨慎的态度工作,以解决可能出现的任何问题。”
另一位医疗器械领域资深人士表示,美国FDA在批准创新医疗器械方面一直走在前列,鼓励创新器械的上市,但产品上市后会进行非常严格的不良事件的监测,一旦发现错误会及时召回纠错。
友链
外链
互链
Copyright © 2023 Powered by
六合彩图库源码【购买联系电报bc3979】AC彩票网站源码|六合彩源码|彩票搭建|新中原六合彩源码|【网站bc9797.com】六合彩论坛源码【联系飞机bc3979】
sitemap
-
文章
8321
-
浏览
93
-
获赞
64837
热门推荐
-
早报:金球奖提名9月7日0点30公布
【金球奖提名时间公布】谁能入选?官方:金球奖提名将于北京时间9月7日0点30公布 官方消息,今年的金球奖提名将于当地时间9月6日下午6:30北京时间9月7日00:30)公布。目前指数方面梅西和哈兰德遥胡萝卜有几种颜色 胡萝卜的常见品种
胡萝卜有几种颜色 胡萝卜的常见品种时间:2022-05-19 12:41:31 编辑:nvsheng 导读:胡萝卜是一种我们大家都很熟悉的蔬菜,同时我们也都知道胡萝卜的颜色,但实际上胡萝卜并不只有蛙泳可以瘦腿吗 轻松拥有迷人美腿
蛙泳可以瘦腿吗 轻松拥有迷人美腿时间:2022-05-20 12:43:46 编辑:nvsheng 导读:蛙泳是可以瘦腿的,并且效果还不错,因为蛙泳在游的过程中非常需要腿部的力量,所以想要瘦腿的朋谈恋爱不是玩心机 这5个方法让你获得他的真心
谈恋爱不是玩心机 这5个方法让你获得他的真心时间:2022-05-19 12:45:39 编辑:nvsheng 导读:或许防备心太重,或许对自己不够有自信,或许在恋爱中受过的伤太多了...太多的原电讯报:担心沙特拖欠转会费,欧洲俱乐部希望FIFA制定法规保障
9月7日讯 据《每日电讯报》报道,由于担心沙特俱乐部拖欠转会费,欧洲俱乐部希望国际足联制定法规以提供保障,将沙特俱乐部纳入监管中。本周三,包括BIG6在内的英超俱乐部参加了关于欧洲足球未来的闭门会谈。有助于缓解牙齿疼痛的快速办法
有助于缓解牙齿疼痛的快速办法时间:2022-05-20 12:36:54 编辑:nvsheng 导读:牙齿疼痛怎么办?有怎么方法能治疗牙痛?牙痛困扰着许多人,有时疼痛的难受去医院,要做好牙齿不痛得勇敢再爱一次 别让情伤成为你幸福的绊脚石
勇敢再爱一次 别让情伤成为你幸福的绊脚石时间:2022-05-19 12:45:18 编辑:nvsheng 导读:情伤总让人心碎甚至不相信爱情。但你其实偷偷希望再度爱人与被爱,只是没有勇气再踏出去香港冬天穿什么衣服 香港冬天穿羽绒服吗
香港冬天穿什么衣服 香港冬天穿羽绒服吗时间:2022-05-20 12:40:59 编辑:nvsheng 导读:香港的温度差距不像我国北方那么多,位于亚热带地区的香港一年四季气候都相对较高。那么,《宣誓》总监不担心夹在《刺客信条:影》和《怪物猎人:荒野》之间发售
由于今年Xbox第一方游戏扎堆,2A游戏《宣誓》被微软强行延后到了明年2月19日,但这样以来黑曜石这款《上古卷轴:天际》类RPG就会面临外部游戏的强烈竞争,包括Capcom的《怪物猎人:荒野》2月28小满之后为什么没有大满 原来是这样
小满之后为什么没有大满 原来是这样时间:2022-05-20 12:39:06 编辑:nvsheng 导读:在24节气的小满之后没有大满,而是直接到芒种,可能很多人都不太理解其中的原因,这个是和小快快乐乐瘦身你需要有什么样的心理
快快乐乐瘦身你需要有什么样的心理时间:2022-05-19 12:44:57 编辑:nvsheng 导读:杂志、网路、SNS社群网站等等,到处都有人分享瘦身减肥的经验和方法。撑不到最后,结果还是瘦核桃真的能补脑吗 核桃可以补肾吗
核桃真的能补脑吗 核桃可以补肾吗时间:2022-05-19 12:45:00 编辑:nvsheng 导读:核桃是我们都非常熟悉的一种坚果,同时我们也都听说过核桃是可以补脑的,但是很少有人知道核桃补adidas Ultra Boost 鞋款全新“Washington Huskies”配色释出
潮牌汇 / 潮流资讯 / adidas Ultra Boost 鞋款全新“Washington Huskies”配色释出2019年08月28日浏览:3538 不久前,a2018元旦会下雨吗 2018年元旦天气怎么样
2018元旦会下雨吗 2018年元旦天气怎么样时间:2022-05-19 12:43:43 编辑:nvsheng 导读:元旦很多人都会计划出去游玩,因此,天气情况是人们关注的焦点之一。那么,2012018日本福袋什么时候出 2018日本福袋攻略
2018日本福袋什么时候出 2018日本福袋攻略时间:2022-05-20 12:40:31 编辑:nvsheng 导读:早在前几个月,各大品牌都开始纷纷推出新年福袋,抢占新年市场,这个已经是每年
 科技创新!
科技创新!